3.1. Aminoácidos: unidad básica de las proteínas
Las proteínas son las moléculas más versátiles del organismo. Catalizan reacciones, transportan oxígeno, defienden frente a infecciones, transmiten señales y forman estructuras. Toda esta diversidad funcional se construye a partir de una unidad básica común: el aminoácido.
Un aminoácido es una molécula orgánica que contiene al menos un grupo amino (–NH₂) y un grupo carboxilo (–COOH). Los aminoácidos que forman las proteínas son todos α-aminoácidos: ambos grupos funcionales están unidos al mismo carbono, denominado carbono α.
La estructura general de un α-aminoácido tiene cuatro elementos unidos al carbono α:
- Un grupo amino (–NH₂)
- Un grupo carboxilo (–COOH)
- Un átomo de hidrógeno (–H)
- Una cadena lateral o radical (–R), distinta en cada aminoácido
El carbono α es un carbono asimétrico en todos los aminoácidos excepto en la glicina, cuya cadena lateral es simplemente un hidrógeno. Esta asimetría genera dos enantiómeros, L y D. Los aminoácidos de las proteínas son casi exclusivamente de la serie L.
Lo que diferencia a un aminoácido de otro no es su esqueleto básico — que es idéntico en todos — sino su cadena lateral –R. La naturaleza química de esa cadena determina las propiedades del aminoácido y su papel en la estructura y función de la proteína.
3.2. Cadena lateral o radical
Existen 20 aminoácidos proteicos estándar, codificados por el código genético. Se clasifican según las propiedades químicas de su cadena lateral, que determinan su comportamiento en la proteína y su interacción con el entorno acuoso del organismo.
3.2.1. Clasificación por polaridad y carga
Los 20 aminoácidos proteicos estándar comparten el mismo esqueleto α-aminoácido, pero difieren en la naturaleza química de su cadena lateral. Esa diferencia determina si el aminoácido es polar o apolar, si puede ionizarse a pH fisiológico y cómo interacciona con el entorno acuoso del organismo. La clasificación más útil desde el punto de vista estructural y funcional los agrupa en cinco categorías:
| Grupo | Cadena lateral | Carga a pH 7,4 | Aminoácidos | Código de una letra |
|---|---|---|---|---|
| Ácidos | –COOH (ionizado: –COO⁻) | Negativa | Aspartato (Asp), Glutamato (Glu) | D, E |
| Básicos | –NH₂ ionizable | Positiva | Lisina (Lys), Arginina (Arg), Histidina (His) | K, R, H |
| Neutros polares | –OH, –SH, –CONH₂ | Neutra | Serina (Ser), Treonina (Thr), Asparagina (Asn), Glutamina (Gln), Tirosina (Tyr), Cisteína (Cys) | S, T, N, Q, Y, C |
| Apolares alifáticos | Cadena carbonada | Neutra | Glicina (Gly), Alanina (Ala), Valina (Val), Leucina (Leu), Isoleucina (Ile), Metionina (Met), Prolina (Pro) | G, A, V, L, I, M, P |
| Apolares aromáticos | Anillo aromático | Neutra | Fenilalanina (Phe), Triptófano (Trp) | F, W |
Los aminoácidos ácidos (Asp, Glu) participan en enlaces iónicos y en los centros activos enzimáticos.
Los básicos (Lys, Arg, His) aportan carga positiva; la histidina es especialmente versátil porque su pKa (~6) le permite actuar como donador o aceptor de protones a pH fisiológico.
Los neutros polares forman puentes de hidrógeno; la cisteína destaca porque su grupo –SH puede formar puentes disulfuro (–S–S–), el único enlace covalente que estabiliza la estructura terciaria además del esqueleto peptídico.
Los aminoácidos apolares tienden a localizarse en el interior hidrofóbico de las proteínas globulares, alejados del entorno acuoso.
3.2.2. Aminoácidos con propiedades especiales
Varios aminoácidos tienen propiedades estructurales o funcionales que merecen atención específica:
Glicina (Gly, G) es el aminoácido más pequeño — su cadena lateral es un hidrógeno. Esta simplicidad le confiere una flexibilidad conformacional única: aparece con frecuencia en giros y bucles donde se necesita cambiar de dirección en la cadena polipeptídica.
Prolina (Pro, P) es técnicamente un iminoácido: su cadena lateral forma un anillo cíclico que incluye al nitrógeno del grupo amino, convirtiéndolo en una amina secundaria. Esto impide la formación del enlace de hidrógeno típico del grupo –NH y, sobre todo, interrumpe la α-hélice. La prolina actúa como disruptora de estructuras secundarias regulares.
Cisteína (Cys, C) puede oxidarse para formar puentes disulfuro con otra cisteína, generando el aminoácido compuesto cistina. Los puentes disulfuro son los únicos enlaces covalentes que estabilizan la estructura terciaria además del propio esqueleto peptídico.
Aminoácidos aromáticos — fenilalanina, tirosina y triptófano — absorben luz ultravioleta, propiedad que se aprovecha para cuantificar proteínas espectrofotométricamente (absorbancia a 280 nm).
3.2.3. Ionización y punto isoeléctrico
Los grupos amino y carboxilo de los aminoácidos se ionizan en solución acuosa en función del pH. A pH bajo (ácido), predomina la forma catiónica (carga neta positiva); a pH alto (básico), predomina la forma aniónica (carga neta negativa). En un pH intermedio característico de cada aminoácido, la carga neta es cero — es el punto isoeléctrico (pI).
El pI es relevante en técnicas de laboratorio como la electroforesis en gel y la cromatografía de intercambio iónico, que separan proteínas según su carga a un pH determinado.
Las cadenas laterales de los aminoácidos ácidos y básicos tienen sus propios valores de pKa, distintos de los del esqueleto α-amino y α-carboxilo. El pI de un aminoácido se calcula como la media de los dos pKa que flanquean la forma neutra.
3.3. El enlace peptídico
Cuando dos aminoácidos se unen, el grupo carboxilo (–COOH) del primero reacciona con el grupo amino (–NH₂) del segundo, liberando una molécula de agua. El enlace resultante es un enlace amida secundaria, denominado enlace peptídico.
Esta reacción de condensación es endergónica en condiciones fisiológicas y requiere el acoplamiento con la hidrólisis de ATP — proceso que ocurre en el ribosoma durante la traducción.
3.3.1. Características del enlace peptídico
El análisis cristalográfico por rayos X reveló que el enlace peptídico tiene propiedades estructurales únicas, con consecuencias directas sobre la forma de las proteínas:
| Característica | Descripción | Consecuencia estructural |
|---|---|---|
| Seis átomos coplanarios | Los átomos Cα–C=O–N–H–Cα forman un plano rígido (plano de la amida) | Define unidades rígidas repetidas a lo largo de la cadena |
| Carácter parcial de doble enlace | El par de electrones del N se deslocaliza sobre C=O (híbridos de resonancia). Longitud C–N: 1,33 Å (intermedia entre simple y doble) | Confiere rigidez al enlace C–N |
| Rigidez sin rotación | No existe rotación libre alrededor del enlace C–N peptídico | Limita los grados de libertad de la cadena a los ángulos φ y ψ del Cα |
| Configuración trans predominante | Los dos Cα quedan en lados opuestos del plano de la amida | Minimiza el impedimento estérico entre cadenas laterales. La configuración cis solo aparece antes de prolina |
| Rotación libre en Cα | Los ángulos φ (N–Cα) y ψ (Cα–C) sí pueden rotar | Son los responsables de la flexibilidad conformacional y de las estructuras secundarias |
La rigidez del enlace peptídico no inmoviliza la proteína, limita los grados de libertad a los ángulos φ y ψ del carbono α. Son precisamente estas restricciones las que hacen posible la formación de estructuras secundarias regulares como la α-hélice y la hoja β.
3.4. Péptidos, polipéptidos y proteínas
La unión sucesiva de aminoácidos mediante enlaces peptídicos genera cadenas de longitud variable. La terminología convencional las clasifica por el número de residuos:
Un dipéptido contiene dos aminoácidos; un tripéptido, tres. Las cadenas de hasta ~15 aminoácidos se denominan oligopéptidos; las de 15 a 50, polipéptidos; y las de más de 50, proteínas. En la práctica, el término «proteína» se usa para cualquier cadena polipeptídica biológicamente funcional, independientemente de su longitud exacta.
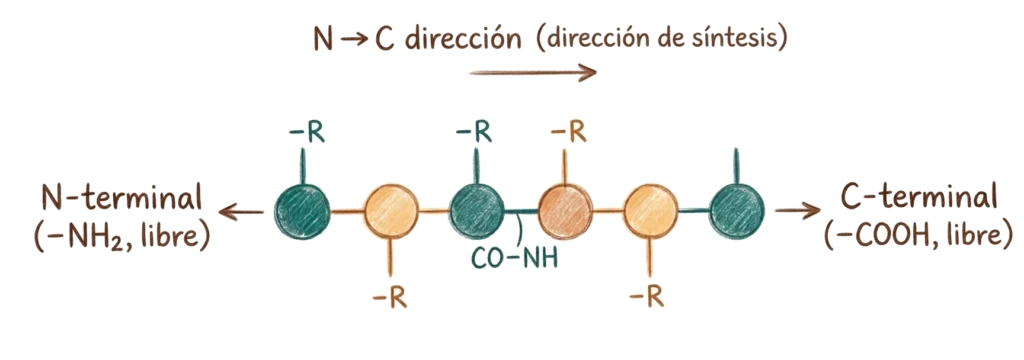
Toda cadena polipeptídica tiene dos extremos diferenciados: el extremo N-terminal, donde el grupo amino del primer aminoácido queda libre, y el extremo C-terminal, donde queda libre el grupo carboxilo del último. Por convención, las secuencias proteicas se escriben y leen siempre en dirección N→C, que es también la dirección de síntesis en el ribosoma.
El esqueleto de la cadena — los átomos repetidos de N–Cα–C a lo largo de toda la proteína — es común a todos los residuos. Lo que varía en cada posición son las cadenas laterales, que sobresalen del esqueleto y son las que confieren a cada proteína su identidad química.
3.5. Estructura primaria de las proteínas
La estructura primaria de una proteína es la secuencia lineal y ordenada de sus aminoácidos, unidos mediante enlaces peptídicos, con una direccionalidad N→C definida. Es el primer y más fundamental nivel de organización estructural de las proteínas.
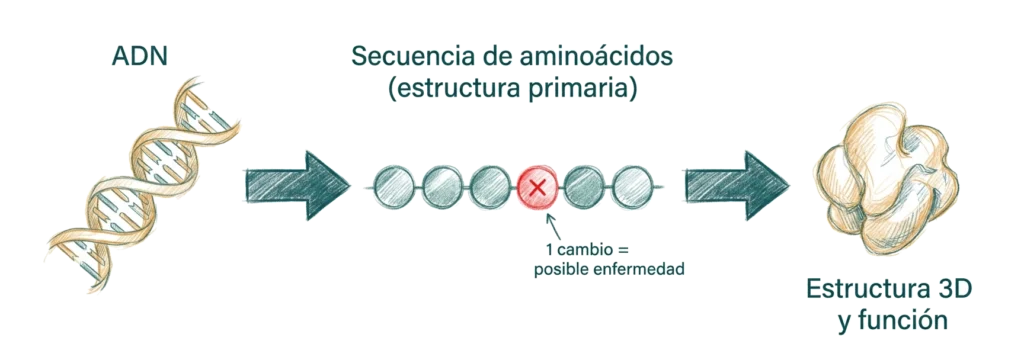
La estructura primaria está codificada directamente en el ADN: la secuencia de nucleótidos determina la secuencia de aminoácidos a través del código genético y del proceso de traducción. En este sentido, la estructura primaria es la traducción molecular del genotipo.
La importancia de la estructura primaria va mucho más allá de ser una simple lista de aminoácidos. La secuencia determina la estructura — los patrones de aminoácidos hidrofóbicos e hidrofílicos, la presencia de prolinas y glicinas, la posición de las cisteínas — y la estructura determina la función. Un cambio en un solo aminoácido puede ser suficiente para alterar radicalmente la función de una proteína.
La anemia falciforme es el ejemplo clásico de enfermedad monogénica causada por un error en la estructura primaria. La hemoglobina S difiere de la hemoglobina A normal en un único aminoácido de la cadena β: la sustitución de glutamato (Glu) — polar, cargado negativamente — por valina (Val) — apolar, hidrofóbico — en la posición 6.
Este cambio crea una zona hidrofóbica en la superficie de la hemoglobina desoxigenada que promueve la polimerización de las moléculas entre sí, formando fibras rígidas que deforman el eritrocito dándole la forma de hoz característica. Los eritrocitos falciformes son frágiles, se destruyen con facilidad (anemia hemolítica) y obstruyen los capilares (crisis vasooclusivas).
Una sola mutación puntual en el ADN → un cambio de aminoácido → una proteína con propiedades físicas alteradas → una enfermedad sistémica grave.
