5.1. El problema del plegamiento
Una proteína recién sintetizada en el ribosoma es una cadena lineal de aminoácidos. Para ser funcional debe alcanzar su conformación nativa: su estructura tridimensional específica, compacta y estable de menor energía. El problema es que una cadena de, por ejemplo, 100 aminoácidos tiene un número astronómico de conformaciones posibles. Si la proteína explorase todas ellas aleatoriamente antes de encontrar la nativa, el proceso tardaría más tiempo del que ha existido el universo. Sin embargo, las proteínas se pliegan en milisegundos o segundos.
Esta contradicción se conoce como la paradoja de Levinthal (1969) y su resolución es que el plegamiento no ocurre por exploración aleatoria sino a través de vías de plegamiento dirigidas: rutas específicas de estados intermedios que conducen de forma eficiente hacia la conformación nativa.
El experimento que estableció el principio fundamental del plegamiento fue realizado por Christian Anfinsen en los años 50-60, trabajando con la ribonucleasa A. Demostró que una proteína completamente desnaturalizada podía recuperar espontáneamente su conformación nativa y su actividad al eliminar el agente desnaturalizante. Esto demostró que toda la información necesaria para el plegamiento está contenida en la secuencia de aminoácidos, en su estructura primaria. Anfinsen recibió el Nobel de Química en 1972.
La secuencia de aminoácidos determina la conformación nativa. El plegamiento es termodinámicamente espontáneo (la conformación nativa es la de menor energía libre), pero ocurre a través de vías intermedias, no por exploración aleatoria.
5.2. Plegamiento no asistido
En condiciones experimentales simplificadas — proteína diluida, temperatura fisiológica, ausencia de agentes desnaturalizantes — muchas proteínas pequeñas pueden plegarse espontáneamente sin la intervención de otras proteínas. Este proceso se denomina plegamiento no asistido.
Dos modelos describen el mecanismo, no necesariamente excluyentes:
5.2.1. Modelo jerarquizado
El plegamiento ocurre de forma secuencial, de estructuras simples a complejas. Tras la síntesis de la estructura primaria, se forman primero los elementos de estructura secundaria local (α-hélices y hojas β) en regiones donde la secuencia lo favorece. Estos elementos actúan como núcleos de plegamiento y, a continuación, las interacciones entre ellos van consolidando la estructura terciaria progresivamente.
5.2.2. Modelo de colapso espontáneo y glóbulo fundido
La cadena polipeptídica lineal sufre un colapso hidrofóbico espontáneo: los residuos apolares, en contacto con el agua, tienden a agruparse rápidamente en el interior, colapsando la cadena en una estructura compacta pero aún desordenada. El resultado es el glóbulo fundido (molten globule).
El glóbulo fundido es un estado intermedio con propiedades características: tiene la estructura secundaria propia de la proteína nativa, pero las interacciones terciarias entre cadenas laterales son todavía incorrectas o inexistentes. El núcleo hidrofóbico existe pero no está consolidado. Desde este estado, la proteína realiza ajustes progresivos hasta alcanzar la conformación nativa.
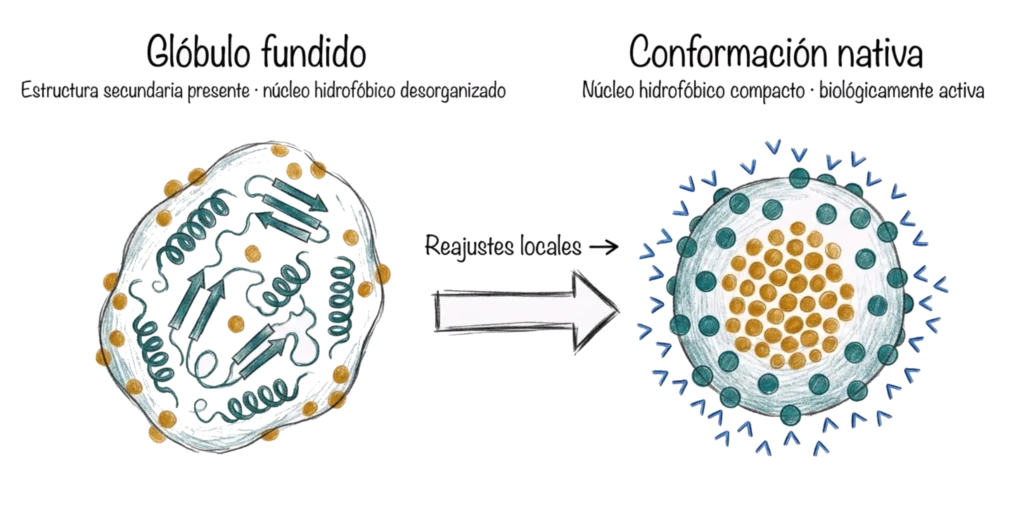
En la práctica, el plegamiento real combina elementos de ambos modelos. Los puntos de iniciación de estructura secundaria actúan como nucleadores, el colapso hidrofóbico compacta la cadena rápidamente generando el glóbulo fundido, y desde ahí los reajustes locales llevan a la conformación nativa.
5.3. Plegamiento asistido: chaperonas
En el interior de una célula viva el plegamiento espontáneo tiene un problema serio: la concentración de proteínas en el citoplasma es extraordinariamente alta (~300 mg/ml). En este entorno denso, las cadenas polipeptídicas recién sintetizadas — con segmentos hidrofóbicos expuestos — tienden a agregarse con otras cadenas antes de terminar de plegarse. La agregación produce estructuras no funcionales e insolubles que pueden ser tóxicas para la célula.
Las chaperonas son proteínas cuya función es prevenir este plegamiento incorrecto y la agregación. Reconocen y se unen a segmentos hidrofóbicos expuestos en cadenas no plegadas o parcialmente plegadas, impidiendo interacciones inapropiadas con otras proteínas.
| Chaperona | Localización | Mecanismo de acción | Dependencia de ATP |
|---|---|---|---|
| Hsp70 (DnaK en E. coli) | Citosol, retículo endoplásmico, mitocondria | Se une a segmentos hidrofóbicos expuestos de cadenas en síntesis o estrés. Ciclos de unión/liberación dan oportunidades de plegamiento | Sí — la hidrólisis de ATP regula la afinidad por el sustrato |
| Hsp40 (DnaJ en E. coli) | Citosol | Cofactor de Hsp70. Estimula la actividad ATPasa de Hsp70 y presenta sustratos | Indirecta (estimula la hidrólisis de ATP de Hsp70) |
| Chaperoninas (GroEL-GroES / TRiC-CCT) | Citosol bacteriano / citosol eucariota | Forman una cámara de plegamiento aislada donde la proteína se pliega sin riesgo de agregación | Sí — ciclos de ATP impulsan los cambios conformacionales del barril |
| Proteína disulfuro isomerasa (PDI) | Retículo endoplásmico | Cataliza la formación e intercambio de puentes disulfuro hasta establecer las combinaciones correctas | No — enzima catalítico |
| Peptidil-prolil cis-trans isomerasa (PPI) | Citosol y retículo endoplásmico | Cataliza la isomerización cis-trans del enlace peptídico antes de residuos de prolina | No — enzima catalítico |
Las chaperonas no aportan información sobre la conformación final de la proteína — esa información sigue estando en la secuencia. Su función es proporcionar el entorno y el tiempo necesarios para que la proteína se pliegue correctamente por sí misma.
5.3.1. Hsp70
Las Hsp70 (heat shock proteins de 70 kDa) son chaperonas ubicuas presentes en todos los organismos. Su nombre refleja que su expresión aumenta en respuesta al estrés térmico, aunque también funcionan en condiciones normales.
Actúan principalmente sobre cadenas polipeptídicas en síntesis en el ribosoma. Se unen a segmentos hidrofóbicos de 7-8 residuos que quedan expuestos durante la síntesis — segmentos que en la proteína nativa quedarían enterrados en el interior. Esta unión impide la agregación y mantiene la cadena en un estado competente para plegarse cuando la síntesis se complete.
La unión y liberación de la cadena sustrato por Hsp70 es un proceso dependiente de ATP: la hidrólisis de ATP promueve cambios conformacionales en la chaperona que alternan entre un estado de alta afinidad (ADP unido, cadena sujeta) y un estado de baja afinidad (ATP unido, cadena liberada). Cada ciclo de unión-liberación da a la cadena una nueva oportunidad de plegarse correctamente.
5.3.2. Chaperoninas
Las chaperoninas son complejos proteicos de gran tamaño que forman una cámara de plegamiento aislada donde una proteína puede completar su plegamiento sin riesgo de agregarse con otras cadenas del citoplasma.
El sistema más estudiado es el complejo GroEL-GroES de E. coli:
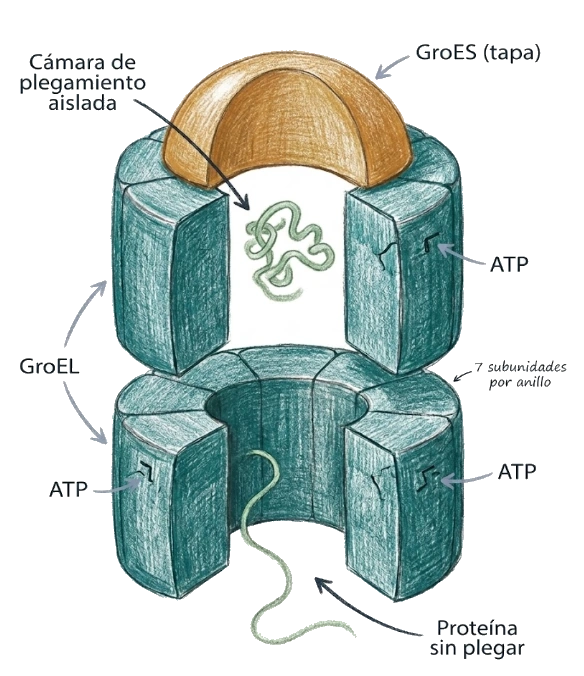
GroEL forma un barril de doble anillo, con siete subunidades por anillo. Cada anillo tiene una cavidad central hidrofóbica que puede alojar una proteína no plegada. GroES actúa como tapa que sella la cavidad de uno de los anillos, creando una cámara aislada donde la proteína queda encerrada.
En el interior de esta cámara, la proteína se plega en condiciones óptimas. La cavidad es hidrofílica y aísla la cadena del citoplasma. El proceso es dependiente de ATP: varios ciclos de unión de ATP, hidrólisis y liberación de GroES permiten repetir el proceso hasta que la proteína alcanza su conformación nativa.
En eucariotas, el equivalente funcional es el complejo TRiC/CCT, presente en el citosol y especialmente importante para el plegamiento de proteínas del citoesqueleto como actina y tubulina.
5.3.3. Enzimas del plegamiento
Además de las chaperonas, existen enzimas específicas que catalizan pasos que de otro modo serían lentos en el plegamiento:
- La proteína disulfuro isomerasa (PDI) cataliza la formación y el reordenamiento de puentes disulfuro. En el plegamiento espontáneo, los puentes disulfuro pueden formarse entre cisteínas incorrectas. La PDI rompe y reforma estos enlaces hasta establecer las combinaciones correctas. Opera en el retículo endoplásmico, donde el entorno oxidante favorece la formación de puentes disulfuro.
- La peptidil-prolil cis-trans isomerasa (PPI) cataliza la isomerización del enlace peptídico antes de los residuos de prolina entre las configuraciones cis y trans. Este paso es intrínsecamente lento en ausencia del enzima y puede ser limitante en el plegamiento de proteínas ricas en prolina.
5.4. Desnaturalización
5.4.1. Concepto y causas
La desnaturalización es la pérdida de la conformación nativa de una proteína como consecuencia de la ruptura de las interacciones que la estabilizan. Implica la desorganización de la estructura secundaria y terciaria (y de la cuaternaria si existe), pero nunca la ruptura de la estructura primaria: los enlaces peptídicos permanecen intactos. Si se rompen los enlaces peptídicos, hablamos de hidrólisis, no de desnaturalización.
Los principales agentes desnaturalizantes son:
| Agente | Mecanismo | Reversibilidad | Ejemplo |
|---|---|---|---|
| Temperatura elevada | Ruptura de interacciones débiles (puentes de H, Van der Waals, hidrofóbicas) | Generalmente irreversible — las cadenas se agregan | Cocción del huevo; esterilización por calor |
| Cambios bruscos de pH | Alteración de cargas en cadenas laterales ionizables → ruptura de enlaces iónicos y puentes de H | Variable según proteína y magnitud del cambio | Precipitación de proteínas plasmáticas en pH extremo |
| Detergentes (SDS) | Disrumpen interacciones hidrofóbicas recubriendo los segmentos apolares | Parcialmente reversible al eliminar el detergente | Electroforesis SDS-PAGE |
| Agentes caotrópicos (urea, GdnHCl) | Compiten con los puentes de hidrógeno intramoleculares | Reversible si se elimina por diálisis | Experimento de Anfinsen con ribonucleasa |
| Agentes reductores (β-ME, DTT) | Rompen puentes disulfuro (–S–S– → 2×–SH) | Reversible al reoxidar en condiciones adecuadas | Desnaturalización completa de ribonucleasa con urea + β-ME |
5.4.2. Reversibilidad: renaturalización
En algunos casos, al eliminar el agente desnaturalizante, la proteína puede recuperar espontáneamente su conformación nativa y su actividad biológica. Este proceso se denomina renaturalización.
El ejemplo clásico es la ribonucleasa A de Anfinsen: al desnaturalizarla completamente con urea y β-mercaptoetanol (que rompe los cuatro puentes disulfuro) y eliminar después ambos agentes por diálisis, la proteína recupera espontáneamente su conformación nativa con los cuatro puentes disulfuro en las posiciones correctas y su actividad enzimática completa. Esta reversibilidad confirmó que toda la información del plegamiento está en la secuencia.
En condiciones fisiológicas, la desnaturalización suele ser irreversible porque las cadenas desnaturalizadas se agregan rápidamente con otras proteínas, formando precipitados insolubles que no pueden recuperarse. El ejemplo cotidiano es la cocción del huevo: la clara coagula de forma irreversible por desnaturalización y agregación de las proteínas del albumen.
5.4.3. Relevancia clínica
La desnaturalización y el plegamiento incorrecto tienen consecuencias clínicas directas.
Un grupo creciente de enfermedades se origina por el plegamiento incorrecto de proteínas específicas que forman agregados insolubles tóxicos denominados amiloides o cuerpos de inclusión. Entre ellas:
- Enfermedad de Alzheimer: acumulación de placas de β-amiloide (proteína Aβ) y ovillos neurofibrilares de proteína tau hiperfosforilada en el parénquima cerebral.
- Enfermedad de Parkinson: agregados de α-sinucleína formando los cuerpos de Lewy en neuronas dopaminérgicas.
- Fibrosis quística: la mutación ΔF508 en la proteína CFTR produce un plegamiento incorrecto que impide su tráfico a la membrana plasmática — la proteína es degradada antes de llegar a su destino.
- Enfermedades priónicas (Creutzfeldt-Jakob, kuru, scrapie): la proteína priónica normal (PrPᶜ) se convierte en una forma mal plegada (PrPˢᶜ) con predominio de hoja β, que actúa como molde para convertir otras moléculas de PrPᶜ. Es el único agente infeccioso conocido sin ácido nucleico.
