4.1. Introducción: de la secuencia a la forma
La estructura primaria de una proteína (su secuencia de aminoácidos) contiene toda la información necesaria para que la cadena polipeptídica adquiera su forma tridimensional funcional. Pero entre la secuencia lineal y la proteína activa hay varios niveles de organización estructural, cada uno construido sobre el anterior.
Se distinguen cuatro niveles:
- La estructura secundaria describe el plegamiento local y regular de segmentos de la cadena polipeptídica.
- La estructura terciaria es la disposición tridimensional completa de toda la cadena.
- La estructura cuaternaria aparece cuando varias cadenas se ensamblan en un complejo.
La conformación nativa es la estructura biológicamente activa; la forma que adopta la proteína en condiciones fisiológicas.
La estructura primaria — secuencia de aminoácidos y enlace peptídico — se describe en el T3 — Aminoácidos y péptidos. El plegamiento y la desnaturalización se desarrollan en el T5 — Plegamiento y desnaturalización de proteínas.
4.2. Estructura secundaria
La estructura secundaria es el patrón de plegamiento local y regular que adoptan segmentos de la cadena polipeptídica. Está estabilizada exclusivamente por puentes de hidrógeno entre átomos del esqueleto peptídico — concretamente entre el oxígeno del grupo carbonilo (–C=O) de un residuo y el hidrógeno del grupo amino (–NH) de otro residuo más adelante en la cadena. Las cadenas laterales no participan en estos puentes de hidrógeno.
Existen dos patrones de estructura secundaria predominantes: la α-hélice y la hoja β. Un tercer elemento, el giro β, conecta estos patrones permitiendo cambios de dirección.
4.2.1. La α-hélice
La α-hélice es la estructura secundaria más frecuente en las proteínas globulares y la predominante en las proteínas fibrosas como la α-queratina. El esqueleto polipeptídico se enrolla en espiral alrededor de un eje longitudinal formando una hélice compacta.
Sus características estructurales son:
- El enrollamiento es dextrógiro (sentido de las agujas del reloj visto desde arriba).
- Cada vuelta contiene 3,6 aminoácidos y tiene una altura de 5,4 Å.
- Los puentes de hidrógeno se forman entre el grupo –C=O del residuo n y el grupo –NH del residuo n+4, todos paralelos al eje de la hélice.
- Las cadenas laterales de los aminoácidos quedan dispuestas radialmente hacia el exterior de la hélice.
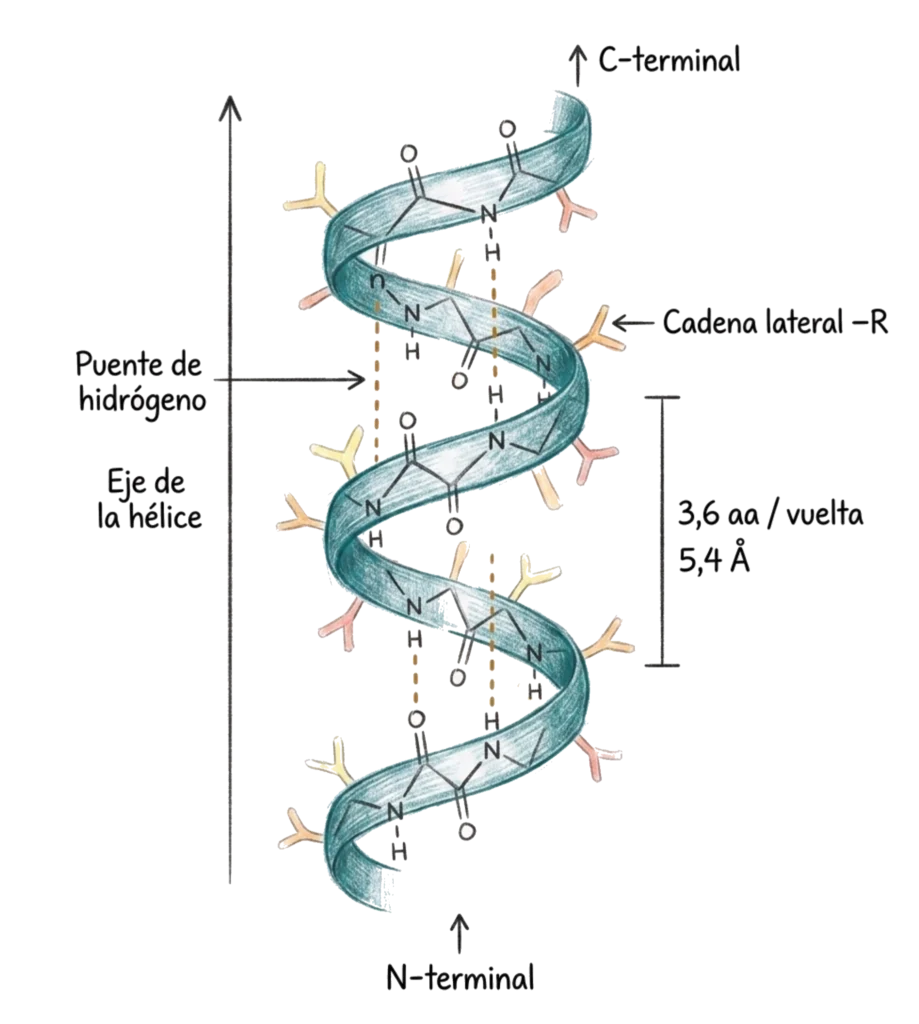
La α-hélice es una estructura local: no toda la proteína está en α-hélice. Es dextrógira, muy compacta, estabilizada por puentes de hidrógeno intracatenarios, y las cadenas laterales quedan fuera.
Factores que impiden o desestabilizan la α-hélice:
- La prolina la interrumpe de forma casi absoluta. Su nitrógeno forma parte de un anillo rígido que impide la geometría necesaria para el puente de hidrógeno y fija el ángulo φ, eliminando la flexibilidad necesaria.
- La glicina la desestabiliza por exceso de flexibilidad. Al tener como cadena lateral solo un hidrógeno, el carbono α de la glicina tiene demasiados grados de libertad conformacionales. La hélice se vuelve inestable porque cualquier perturbación puede deshacerla.
- Las cargas repulsivas entre cadenas laterales adyacentes del mismo signo también impiden su formación. Si varios residuos ácidos o básicos consecutivos se repelen entre sí, la hélice no puede mantenerse.
4.2.2. La hoja β
La hoja β o conformación β es una estructura secundaria más extendida que la α-hélice. La cadena polipeptídica adopta una disposición en zigzag, con las cadenas laterales orientadas alternativamente hacia arriba y hacia abajo del plano.
Lo que da lugar a la hoja β es la superposición lateral de varios segmentos de cadena en zigzag, denominados hebras β, que se estabilizan mediante puentes de hidrógeno entre hebras adyacentes. Según la orientación relativa de las hebras se distinguen dos variantes:
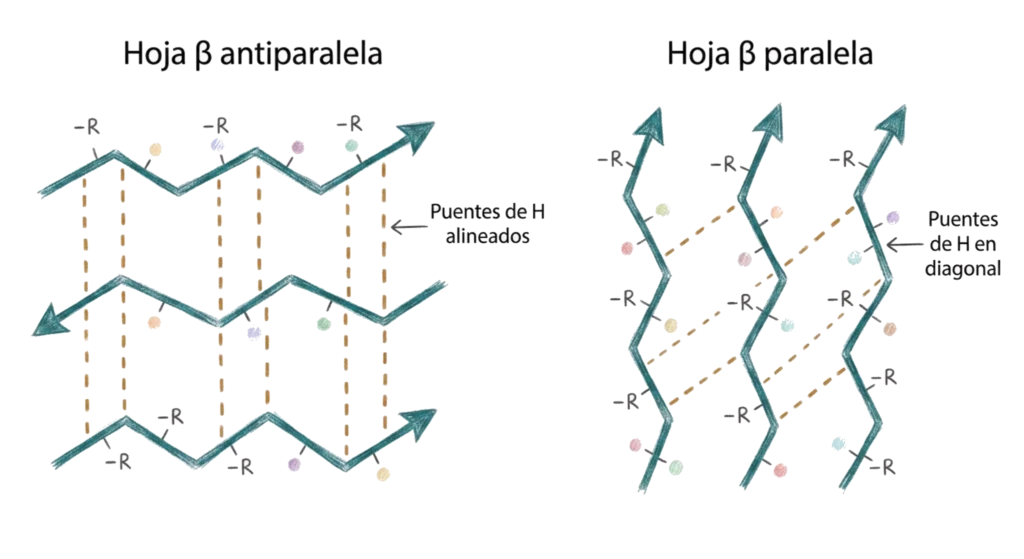
- En la hoja β antiparalela las hebras adyacentes corren en sentidos opuestos (una N→C y la siguiente C→N). Los puentes de hidrógeno están perfectamente alineados y perpendiculares a las hebras — es la variante más estable.
- En la hoja β paralela todas las hebras corren en el mismo sentido (N→C). Los puentes de hidrógeno quedan en diagonal respecto a las hebras — es algo menos estable que la antiparalela.
| Característica | α-hélice | Hoja β |
|---|---|---|
| Tipo de plegamiento | Enrollamiento helicoidal alrededor de un eje | Cadenas en zigzag superpuestas lateralmente |
| Puentes de hidrógeno | Intracatenarios: –C=O del residuo n con –NH del residuo n+4. Paralelos al eje | Intercatenarios: entre hebras adyacentes. Perpendiculares (antiparalela) o en diagonal (paralela) |
| Unidad estructural | 3,6 aminoácidos por vuelta, 5,4 Å de paso | Hebras β de longitud variable |
| Cadenas laterales | Dispuestas radialmente hacia el exterior | Alternativamente arriba y abajo del plano |
| Estabilidad relativa | Alta. Muy compacta | Antiparalela > paralela |
| Ejemplos proteicos | α-queratina, colágeno (variante levógira), mioglobina | Fibroína de seda, dominios β de inmunoglobulinas |
4.2.3. El giro β
El giro β es una estructura secundaria corta que permite a la cadena polipeptídica cambiar de dirección en 180°. Está formado por 4 aminoácidos consecutivos y estabilizado por un puente de hidrógeno entre el primer y el cuarto residuo.
Los giros β son frecuentes en la superficie de las proteínas globulares, donde conectan segmentos de α-hélice o de hoja β. Los aminoácidos glicina y prolina aparecen con frecuencia en estas estructuras: la glicina por su flexibilidad, y la prolina porque puede adoptar la configuración cis del enlace peptídico con relativa facilidad, facilitando el giro de 180°.
4.3. Estructura terciaria
La estructura terciaria es la disposición tridimensional completa de toda la cadena polipeptídica: el resultado de plegar y enrollar los elementos de estructura secundaria (α-hélices, hojas β, giros β y segmentos sin estructura regular) en una conformación tridimensional compacta y específica.
4.3.1. Fuerzas de estabilización
La estructura terciaria se mantiene gracias a la combinación de varios tipos de interacciones entre las cadenas laterales de los aminoácidos:
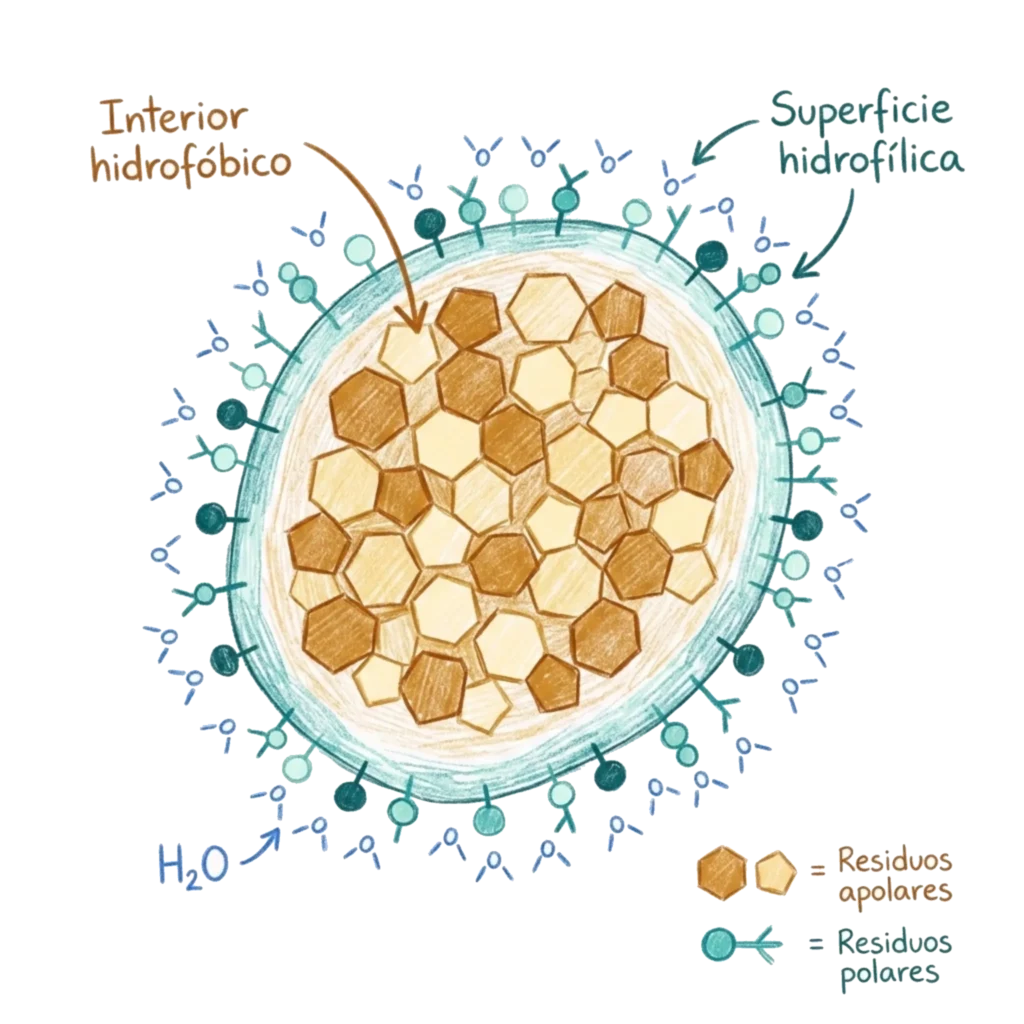
- Las interacciones hidrofóbicas son la fuerza predominante. Los residuos apolares tienden a agruparse en el interior de la proteína, alejados del entorno acuoso. No son enlaces propiamente dichos — son exclusiones entrópicas: el agua excluye a los grupos hidrofóbicos de la superficie, forzándolos al interior.
- Los puentes de hidrógeno entre cadenas laterales polares contribuyen a la estabilidad, especialmente en la superficie de la proteína donde los residuos interaccionan con el agua.
- Los enlaces iónicos (interacciones electrostáticas) se forman entre cadenas laterales de carga opuesta — por ejemplo entre un residuo ácido (Glu, Asp) y uno básico (Lys, Arg).
- Las fuerzas de Van der Waals son débiles individualmente pero contribuyen de forma significativa por su número: en el interior compacto de una proteína hay miles de contactos de Van der Waals.
- Los puentes disulfuro (–S–S–) entre dos residuos de cisteína son los únicos enlaces covalentes que estabilizan la estructura terciaria además del esqueleto peptídico. Son especialmente frecuentes en proteínas extracelulares, donde el entorno oxidante favorece su formación.
| Tipo de interacción | Naturaleza | Localización preferente | Ejemplo |
|---|---|---|---|
| Hidrofóbica | No covalente (entrópica) — los residuos apolares son excluidos por el agua | Interior de la proteína | Agrupación de Val, Leu, Ile en el núcleo |
| Puente de hidrógeno | No covalente (débil) — entre grupos polares | Interior y superficie | Ser, Thr, Asn en contacto con otras cadenas laterales |
| Iónica (electrostática) | No covalente — entre cadenas laterales de carga opuesta | Superficie preferentemente | Glu (–) con Lys (+) |
| Van der Waals | No covalente (muy débil) — entre dipolos transitorios | Interior compacto | Cualquier par de átomos muy próximos |
| Puente disulfuro | Covalente — oxidación de dos grupos –SH | Proteínas extracelulares | Dos residuos de Cys formando –S–S– |
4.3.2. Proteínas globulares y fibrosas
Las proteínas se clasifican estructuralmente en dos grandes grupos según la organización de su estructura terciaria:
Las proteínas fibrosas tienen una estructura alargada, formada por una única estructura secundaria repetida que se superpone o enrolla sobre sí misma. Son insolubles en agua por su alto contenido en residuos hidrofóbicos y tienen función estructural. Ejemplos: α-queratina (pelo, uñas, cuernos — dos α-hélices dextrógiras enrolladas en superhélice levógira), colágeno (tres cadenas en α-hélice levógira muy empaquetada enrolladas en triple hélice dextrógira) y fibroína de seda (hojas β paralelas).
Las proteínas globulares tienen una forma compacta, esférica u ovoide, resultado de combinar distintos tipos de estructura secundaria plegados en una conformación tridimensional específica. Son solubles en agua — los residuos polares quedan en la superficie y los hidrofóbicos en el interior. Tienen función dinámica: catálisis enzimática, transporte, señalización, defensa inmune. Ejemplo prototípico: la mioglobina, formada por 153 aminoácidos y una estructura mayoritariamente en α-hélice.
| Característica | Proteínas fibrosas | Proteínas globulares |
|---|---|---|
| Estructura secundaria | Una única estructura secundaria repetida | Combinación de α-hélices, hojas β y giros β |
| Forma | Alargada, fibrilar | Compacta, esférica u ovoide |
| Solubilidad | Insolubles en agua | Solubles en agua |
| Función | Estructural (soporte mecánico) | Dinámica (catálisis, transporte, señalización, defensa) |
| Residuos en superficie | Mayoritariamente hidrofóbicos | Mayoritariamente hidrofílicos |
| Ejemplos | α-queratina, colágeno, fibroína de seda | Mioglobina, hemoglobina, enzimas, anticuerpos |
4.4. Estructura cuaternaria
La estructura cuaternaria aparece cuando dos o más cadenas polipeptídicas independientes (denominadas subunidades o protómeros) se asocian formando un complejo funcional. Cada subunidad posee su propia estructura terciaria; la estructura cuaternaria describe cómo se ensamblan entre sí.
Las subunidades se mantienen unidas por los mismos tipos de interacciones no covalentes que estabilizan la estructura terciaria: interacciones hidrofóbicas, puentes de hidrógeno, enlaces iónicos y fuerzas de Van der Waals. En algunos casos también participan puentes disulfuro intercatenarios.
Las subunidades pueden ser idénticas (homoméricas) o distintas (heteroméricas), y habitualmente se agrupan en número par.
La hemoglobina está formada por cuatro subunidades: dos cadenas α y dos cadenas β (hemoglobina A del adulto), cada una con su propio grupo hemo. El 60% de su estructura es α-hélice. La estructura cuaternaria permite la cooperatividad en la unión del oxígeno y la regulación alostérica por CO₂, H⁺ y 2,3-bisfosfoglicerato. Ninguna de estas propiedades existe en la subunidad aislada.
No todas las proteínas tienen estructura cuaternaria. La mioglobina es funcional con una sola cadena (estructura terciaria). La hemoglobina necesita cuatro subunidades ensambladas para ejercer su función de transporte cooperativo de oxígeno.
4.5. Conformación nativa
La conformación nativa es la estructura tridimensional biológicamente activa de una proteína en condiciones fisiológicas. De entre todas las conformaciones posibles que podría adoptar una cadena polipeptídica, la nativa es la termodinámicamente más estable: la que tiene la energía libre mínima y el máximo número de interacciones débiles estabilizadoras.
La conformación nativa se caracteriza por tres rasgos estructurales consistentes en todas las proteínas globulares:
- Los residuos hidrofóbicos se localizan en el interior de la molécula, formando un núcleo compacto alejado del agua.
- Los residuos polares e iónicos se sitúan en la superficie, donde interaccionan con el entorno acuoso.
- Se maximiza el número de puentes de hidrógeno intramoleculares posibles.
La conformación nativa no es necesariamente estática. Los enzimas, por ejemplo, pueden sufrir cambios conformacionales reversibles al unirse a su sustrato, pero siempre sin rotura de enlaces covalentes. Lo que define la nativa no es la rigidez, sino ser la conformación activa de menor energía libre.
