4.1. Las moléculas de adhesión celular: visión general
Las células de los organismos multicelulares mantienen dos tipos de relaciones con su entorno: las uniones estructurales estables que forman los complejos de unión y los contactos dinámicos y reversibles mediados por las moléculas de adhesión celular (CAM, del inglés Cell Adhesion Molecules).
Las CAM son proteínas de membrana que reconocen y se unen a moléculas complementarias en células vecinas o en componentes de la matriz extracelular. A diferencia de los complejos de unión, estas interacciones son transitorias: pueden establecerse y romperse en función de las necesidades del momento, lo que las hace esenciales en procesos dinámicos como el desarrollo embrionario, la respuesta inflamatoria, la cicatrización y la migración celular.
Se clasifican en dos grandes grupos según su dependencia del calcio:
- Dependientes de Ca²⁺: cadherinas, selectinas e integrinas. El Ca²⁺ es necesario para mantener la conformación activa de la molécula y su capacidad de unión.
- Independientes de Ca²⁺: familia de las inmunoglobulinas (N-CAM, I-CAM). Funcionan sin necesidad de calcio extracelular.
| Familia | Dependencia Ca²⁺ | Tipo de unión | Ligando | Función principal | Ejemplos |
|---|---|---|---|---|---|
| Cadherinas | Sí | Homofílica (cadherina-cadherina) | Cadherina del mismo tipo en célula vecina | Adhesión célula-célula · organización tisular · desarrollo embrionario | Cadherina E, N, P · desmogleína |
| Selectinas | Sí | Heterofílica (lectina-oligosacárido) | Oligosacáridos específicos en membrana de otra célula | Adhesión transitoria en circulación · extravasación leucocitaria | Selectina L (leucocitos) · P (plaquetas) · E (endotelio) |
| Integrinas | Sí (Ca²⁺ o Mg²⁺) | Heterofílica (integrina-matriz) | Fibronectina · laminina · colágeno · fibrinógeno | Adhesión célula-matriz · señalización bidireccional | α5β1 (fibronectina) · α6β4 (hemidesmosoma) · αIIbβ3 (plaquetas) |
| Familia Ig (CAM) | No | Homofílica o heterofílica | N-CAM con N-CAM · I-CAM con integrinas β2 | Adhesión neuronal · adhesión firme leucocito-endotelio | N-CAM · I-CAM · V-CAM |
4.2. Cadherinas
Las cadherinas son las principales moléculas de adhesión célula-célula. Son glicoproteínas transmembrana monopaso de 700-750 aminoácidos, dependientes de Ca²⁺, que median uniones homofílicas: una cadherina se une a otra cadherina del mismo tipo en la célula vecina.
Su importancia es especialmente notable en el periodo embrionario, donde el reconocimiento selectivo entre células que expresan el mismo tipo de cadherina dirige la organización de los tejidos y la separación de capas germinales.
4.2.1. Cadherinas clásicas
Las cadherinas clásicas son las mejor caracterizadas. Se expresan de forma diferencial según el tipo celular:
- Cadherina E (epitelial): presente en la mayoría de los epitelios. Es la cadherina más estudiada y un marcador de diferenciación epitelial. Su pérdida en células tumorales es un paso clave en la transición epitelio-mesénquima y en la progresión hacia la metástasis.
- Cadherina N (neural): expresada en células musculares, nerviosas y del cristalino. Participa en la formación de contactos entre neuronas durante el desarrollo del sistema nervioso.
- Cadherina P (placentaria): presente en placenta y epidermis.
4.2.2. Cadherinas no clásicas
Las cadherinas no clásicas tienen estructura relacionada pero funciones distintas:
- Cadherinas de los desmosomas: desmogleína y desmocolina, ya descritas en el contexto de los complejos de unión (T3).
- Protocadherinas del cerebro: más de 50 tipos distintos, expresados en el sistema nervioso. Su enorme diversidad contribuye a la especificidad de las conexiones neuronales.
- Cadherina T: no tiene función de adhesión conocida; actúa como receptor de señalización.
4.2.3. Estructura y mecanismo de unión
La parte extracelular de las cadherinas tiene 5-6 dominios con estructura similar a los dominios de inmunoglobulina. Estos dominios forman homodímeros en la membrana de una misma célula (dimerización en cis), y el homodímero resultante se une al homodímero equivalente de la célula vecina (unión en trans).
La unión en trans es dependiente de Ca²⁺: los iones calcio se unen en las uniones entre dominios consecutivos, rigidificando la estructura extracellular y permitiendo la interacción entre células. Sin Ca²⁺, las cadherinas adoptan una conformación flexible e inactiva.
En el citoplasma, las cadherinas clásicas se unen a cateninas (α, β y p120), que conectan la cadherina con los filamentos de actina del citoesqueleto. Esta conexión es esencial para la función de adhesión: cadherinas sin conexión al citoesqueleto no forman uniones funcionales.
La cadherina E actúa como supresor de tumores: mantiene a las células epiteliales unidas e inhibe su migración. En muchos carcinomas, la pérdida de expresión de cadherina E por metilación del promotor o mutación permite que las células tumorales se separen del tumor primario, invadan el tejido circundante y alcancen los vasos para producir metástasis. La pérdida de cadherina E es uno de los marcadores de mal pronóstico más estudiados en oncología.
4.3. Selectinas
Las selectinas son glicoproteínas de membrana dependientes de Ca²⁺ que pertenecen a la familia de las lectinas: proteínas capaces de unirse a azúcares específicos. A diferencia de las cadherinas, median uniones heterofílicas: la selectina reconoce y se une a un oligosacárido específico en la membrana de otra célula, no a otra selectina.
Sus uniones son más débiles y transitorias que las de las cadherinas, lo que las hace especialmente adecuadas para mediar contactos dinámicos en el torrente circulatorio.
Existen tres tipos según la célula que las expresa:
- Selectina L (leucocitaria): expresada en leucocitos. Media la adhesión inicial de los leucocitos a la pared del vaso.
- Selectina P (plaquetaria): expresada en plaquetas y células endoteliales activadas. Se almacena en gránulos intracelulares y se moviliza rápidamente a la membrana tras la activación.
- Selectina E (endotelial): expresada en células endoteliales activadas por citocinas inflamatorias.
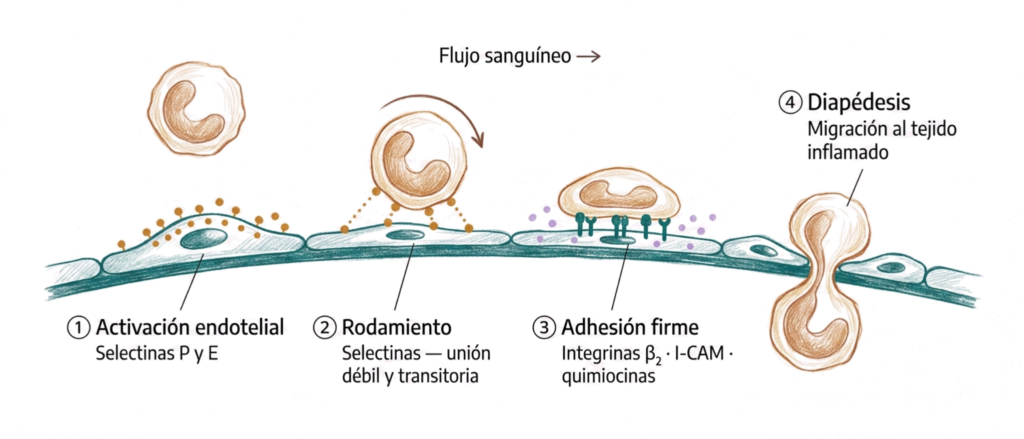
El papel central de las selectinas es en la extravasación leucocitaria: el proceso por el que los leucocitos salen del torrente circulatorio y migran al tejido inflamado.
La extravasación leucocitaria ocurre en tres pasos secuenciales.
- Las selectinas median el rodamiento del leucocito sobre el endotelio activado: uniones débiles y transitorias que ralentizan el leucocito sin detenerlo.
- Segundo, quimiocinas en la superficie endotelial activan las integrinas del leucocito.
- Tercero, las integrinas activadas median la adhesión firme al endotelio y la posterior diapédesis hacia el tejido.
4.4. Integrinas
Las integrinas son las principales moléculas de adhesión célula-matriz extracelular, aunque en algunos contextos también median uniones célula-célula, especialmente en células sanguíneas.
Son proteínas transmembrana muy numerosas en la superficie celular, pero con baja afinidad individual por sus ligandos. Esta característica es funcionalmente relevante: permite uniones reversibles y regulables. La unión fuerte se logra por cooperatividad: múltiples integrinas actuando simultáneamente generan una adhesión global intensa.
4.4.1. Estructura
Las integrinas son heterodímeros formados por dos subunidades glicoproteicas transmembrana asociadas de forma no covalente: la subunidad α y la subunidad β.
Se conocen 29 subunidades α y 9 subunidades β en humanos, que se combinan formando al menos 24 heterodímeros distintos, cada uno con especificidad de unión propia.
La parte extracelular contiene dominios de unión a iones divalentes (Ca²⁺ o Mg²⁺ según el heterodímero) que son necesarios para la unión al ligando.
Las subunidades β más relevantes son:
- β₁: presente en casi todas las células. Se combina con al menos 12 subunidades α distintas. Media la unión a componentes de la matriz extracelular (fibronectina, laminina, colágeno).
- β₂: interviene principalmente en interacciones célula-célula en el contexto de las células sanguíneas. Se combina con al menos 4 subunidades α.
- β₃: presente en plaquetas y otros tipos celulares. Media la unión al fibrinógeno y otras proteínas de la matriz, siendo esencial en la agregación plaquetaria.
La mayoría de las integrinas se conectan en el citoplasma a los filamentos de actina mediante proteínas de anclaje como talina, α-actinina y filamina. La excepción es la integrina α₆β₁, presente en los hemidesmosomas, que se conecta a filamentos intermedios a través de plectina.
| Subunidad β | Distribución celular | Ligandos principales | Función destacada |
|---|---|---|---|
| β₁ | Presente en casi todas las células | Fibronectina · laminina · colágeno | Unión a matriz extracelular · se combina con al menos 12 subunidades α |
| β₂ | Células sanguíneas (leucocitos) | I-CAM · otras proteínas de superficie | Interacciones célula-célula en inflamación · extravasación leucocitaria |
| β₃ | Plaquetas · células endoteliales · otros | Fibrinógeno · vitronectina · fibronectina | Agregación plaquetaria · señalización inside-out en activación plaquetaria |
| β₄ | Células epiteliales basales | Laminina de la membrana basal | Hemidesmosomas · anclaje epitelio-membrana basal (junto con α₆) |
4.4.2. Señalización bidireccional
Una propiedad fundamental que distingue a las integrinas de otras moléculas de adhesión es su capacidad de señalizar en ambas direcciones:
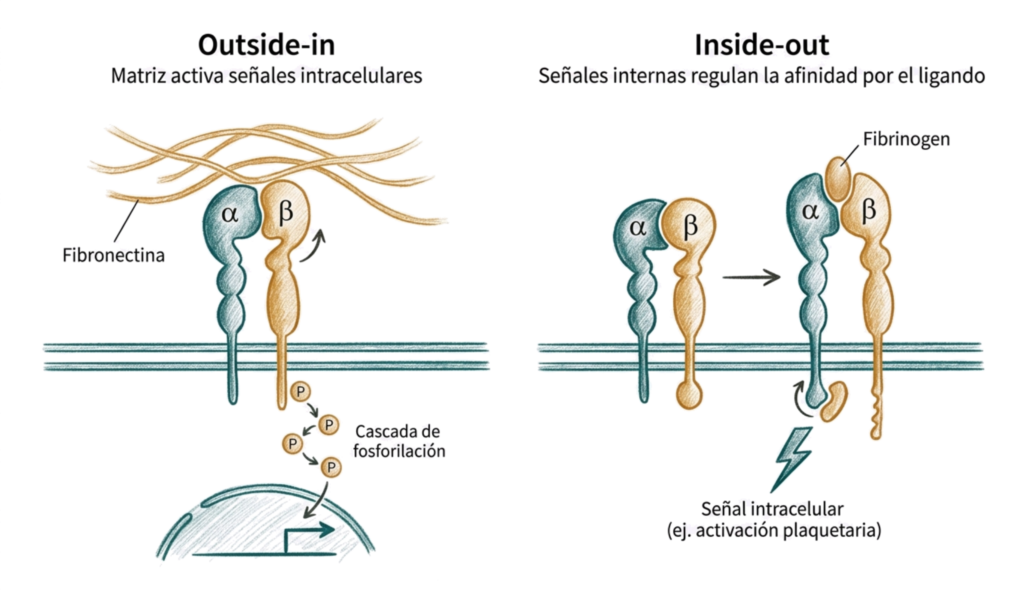
- Señalización de fuera a dentro (outside-in): la unión de la integrina a su ligando en la matriz extracelular desencadena cascadas de fosforilación intracelular que pueden modificar la proliferación, la supervivencia, la diferenciación y la migración celular. La integrina actúa como receptor que traduce información mecánica de la matriz en señales bioquímicas.
- Señalización de dentro a fuera (inside-out): señales generadas en el interior de la célula pueden modificar la conformación de la integrina en la cara extracelular, aumentando o disminuyendo su afinidad por el ligando. Este mecanismo es esencial en la activación plaquetaria: en reposo, la integrina β₃ tiene baja afinidad por el fibrinógeno; tras la activación plaquetaria, señales intracelulares aumentan su afinidad, permitiendo la agregación.
4.5. Familia de las inmunoglobulinas: N-CAM e I-CAM
La familia de las inmunoglobulinas agrupa proteínas de adhesión independientes de Ca²⁺ que contienen uno o más dominios Ig en su parte extracelular. La adhesión que proporcionan es generalmente más débil que la mediada por cadherinas.
Las más relevantes son:
- N-CAM (Neural Cell Adhesion Molecule): media uniones homofílicas (N-CAM con N-CAM) en el sistema nervioso, donde participa en la formación y estabilización de conexiones neuronales. Existen al menos 20 isoformas distintas generadas por splicing alternativo. Algunas contienen grandes cantidades de ácido siálico que, por su carga negativa, reducen la adhesión: la expresión de isoformas con mucho ácido siálico en el tejido nervioso embrionario mantiene los contactos poco estables, favoreciendo la plasticidad necesaria para el crecimiento axonal.
- I-CAM (Intercellular Adhesion Molecule): expresada en células endoteliales. Media uniones heterofílicas con las integrinas β₂ de los leucocitos. Es la molécula que permite la adhesión firme del leucocito al endotelio durante la extravasación, completando el proceso iniciado por las selectinas.
4.6. Interacción con la matriz extracelular
Las moléculas de adhesión no solo conectan células entre sí: también anclan las células a la matriz extracelular, el entramado de proteínas y polisacáridos que ocupa el espacio intercelular en los tejidos.
Las integrinas son los principales receptores de la matriz extracelular. Sus ligandos incluyen fibronectina, laminina, colágeno, vitronectina y fibrinógeno, entre otros. La unión de las integrinas a estos componentes no es solo estructural: transmite al interior celular información sobre la composición, la rigidez y el estado de la matriz, regulando el comportamiento de la célula en respuesta a su entorno físico.
Esta capacidad de las células de «sentir» la matriz a través de las integrinas tiene implicaciones clínicas directas en cicatrización, fibrosis y cáncer.
La composición y función de la matriz extracelular se desarrollan en Histología, en el contexto del tejido conjuntivo. La señalización intracelular desencadenada por integrinas se retoma en los temas de señalización celular de Bioquímica.
