4.1. La membrana plasmática: estructura y modelo
4.1.1. El modelo de mosaico fluido
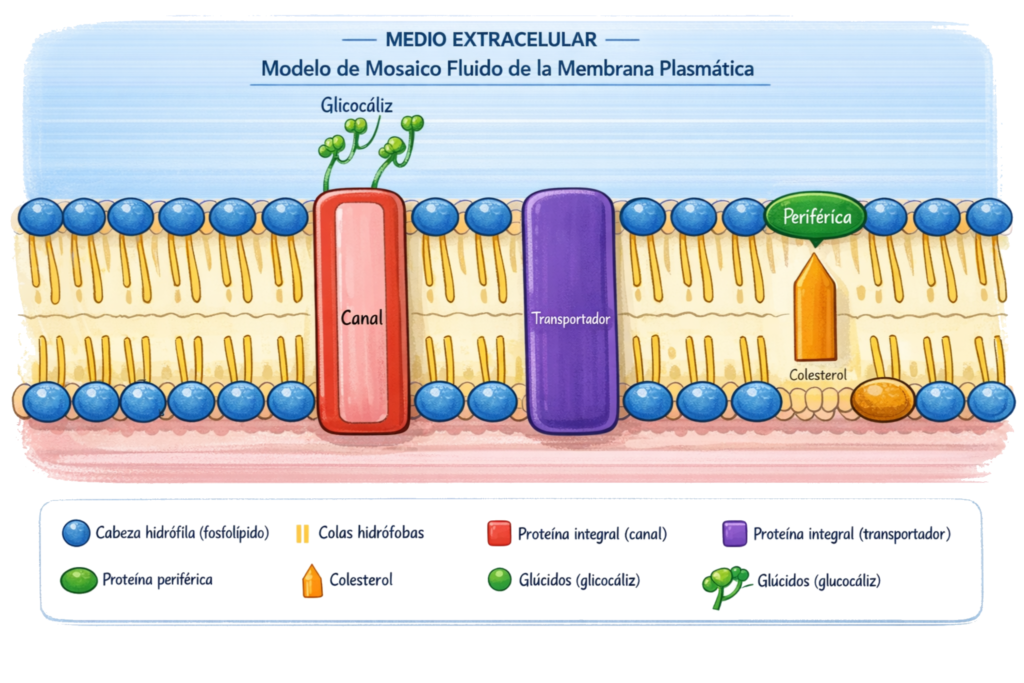
La membrana plasmática es una estructura dinámica que delimita la célula y separa el medio intracelular del extracelular. El modelo clásico que la describe es el modelo de mosaico fluido, propuesto por Singer y Nicolson en 1972. Según este modelo, la membrana es una bicapa lipídica en la que se insertan y desplazan lateralmente proteínas de distintos tipos, formando un «mosaico» móvil.
El modelo se ha refinado desde entonces. Hoy sabemos que la membrana no es uniformemente fluida, sino que presenta microdominios organizados llamados balsas lipídicas (lipid rafts), enriquecidos en esfingolípidos y colesterol, que funcionan como plataformas de señalización. Además, el modelo fence-and-picket (Kusumi et al.) describe cómo el citoesqueleto subyacente crea barreras que compartimentalizan la membrana y limitan la difusión libre de sus componentes.
La membrana no es un "mar de lípidos" homogéneo: posee microdominios funcionales (lipid rafts) y está compartimentalizada por el citoesqueleto.
4.1.2. Composición química
La membrana tiene un grosor constante de 7,5 a 10 nm. Su composición, expresada en masa, es la siguiente:
| Componente | % en masa | Función principal |
|---|---|---|
| Proteínas | ~50–55% | Transporte, señalización, reconocimiento, catalíticas |
| Fosfolípidos | ~25% | Estructura de la bicapa, barrera de permeabilidad |
| Colesterol | ~13% | Regulación de la fluidez; estabilidad mecánica |
| Otros lípidos | ~4% | Señalización (fosfatidilserina, esfingolípidos) |
| Glúcidos | ~3% | Glicocáliz: reconocimiento celular, protección |
En términos molares la relación se invierte: hay ~50 moléculas de fosfolípido por cada proteína. Las proteínas pesan mucho más individualmente, de ahí la diferencia.
4.1.2.1. Lípidos de membrana
Los fosfolípidos son moléculas anfipáticas: poseen una cabeza hidrófila (con grupo fosfato) y dos colas hidrófobas (cadenas de ácidos grasos). En medio acuoso se autoorganizan espontáneamente en bicapa, con las colas enfrentadas hacia el interior y las cabezas en contacto con el agua.
El colesterol se intercala entre los fosfolípidos y actúa como regulador de la fluidez: a temperaturas fisiológicas reduce la fluidez excesiva y a bajas temperaturas impide la solidificación. La fosfatidilserina, normalmente en la cara interna, cuando se expone en la cara externa funciona como señal de apoptosis («come-me signal» para macrófagos).
La distribución de fosfolípidos no es igual en ambas capas de la bicapa: la fosfatidilcolina y la esfingomielina predominan la cara externa, mientras que la fosfatidilserina y la fosfatidiletanolamina lo hacen en la cara interna. Esa asimetría es activa y funcionalmente relevante.
Sus aspectos morfológicos se desarrollan en Biología T9 – Membrana celular I. Morfología y organización.
4.1.2.2. Proteínas de membrana
| Tipo | Localización | Características | Ejemplos |
|---|---|---|---|
| Integrales (intrínsecas) | Atraviesan total o parcialmente la bicapa | Para extraerlas hay que romper la membrana (detergentes) | Canales iónicos, transportadores, receptores |
| Periféricas (extrínsecas) | Cara externa o interna, sin atravesar la bicapa | Unidas por enlaces débiles a otras proteínas o lípidos | Espectrina, ankirina, proteínas G |
| Ancladas a lípidos | Unidas covalentemente a un lípido de la bicapa | Anclaje GPI (exterior) o acilación/prenilación (interior) | Fosfatasa alcalina, priones |
4.1.2.3. Glúcidos: el glicocalix o glucocálix
Los glúcidos de membrana (~3% en masa) se encuentran exclusivamente en la cara extracelular, formando el glicocalix. Están unidos a proteínas (glucoproteínas, proteoglicanos) o a lípidos (glucolípidos). El glicocalix cumple funciones de reconocimiento celular (grupos sanguíneos ABO, HLA), protección mecánica, adhesión celular y creación de una atmósfera celular con cargas que interaccionan con el entorno. Puede alcanzar 20 nm de grosor en células como las plaquetas.
Glicocalix o glucocálix: capa de carbohidratos en la superficie externa de la membrana.
Funciones del glucocálix:
- Reconocimiento celular (sistema inmunitario, grupos sanguíneos...)
- Protección
- Adhesión
- Señalización
Las alteraciones del glicocalix pueden desencadenar enfermedades autoinmunes.
4.1.3. Funciones de la membrana plasmática
| Función | Tipo | Descripción |
|---|---|---|
| Aislamiento | Intrínseca | Barrera selectiva entre el medio intra- y extracelular |
| Intercambio selectivo | Intrínseca | Transporte regulado de iones, nutrientes, desechos |
| Reconocimiento celular | Intrínseca | Identificación propia/ajena mediante glicocáliz |
| Transducción de señales | Intrínseca | Receptores que convierten señales extracelulares en intracelulares |
| Movimiento celular | Extrínseca | Seudópodos, lamelipodios (conexión con citoesqueleto) |
| Elasticidad/deformabilidad | Extrínseca | Cambios de forma (ej.: monocito → macrófago tisular) |
| Secreción y excreción | Extrínseca | Liberación de sustancias por exocitosis |
- La membrana tiene 7,5-10 nm de grosor. Composición (en masa): ~55% proteínas, ~25% fosfolípidos, ~13% colesterol, ~3% glúcidos.
- El colesterol regula la fluidez: más colesterol = menos fluidez a temperatura fisiológica.
- La fosfatidilserina en la cara externa es señal de apoptosis.
- Las proteínas integrales necesitan detergentes para ser extraídas; las periféricas se separan con cambios de pH o fuerza iónica.
- El glicocáliz está solo en la cara extracelular
4.2. Permeabilidad de la membrana
La bicapa lipídica es una barrera selectiva. La regla general es que ninguna sustancia hidrófila o cargada atraviesa libremente la bicapa lipídica. Solo pueden cruzarla de forma directa:
- Gases pequeños: O₂, CO₂, NO, N₂ (apolar, pequeño).
- Moléculas apolares pequeñas: etanol, urea, benceno, solventes orgánicos.
- Agua: difunde lentamente a través de la bicapa, pero el flujo fisiológico depende de acuaporinas (canales específicos de agua).
No atraviesan la bicapa: iones (Na⁺, K⁺, Ca²⁺, Cl⁻), azúcares, aminoácidos, nucleótidos, proteínas y cualquier molécula cargada o de gran tamaño. Para estas sustancias son necesarias proteínas de transporte.
Acuaporinas: Familia de canales proteicos específicos para agua (y en algunos casos glicerol). En humanos se han identificado 13 tipos (AQP0-AQP12). Las más relevantes: AQP1 (ubicua), AQP2 (riñón, regulada por ADH/vasopresina), AQP4 (cerebro), AQP5 (pulmón, glándulas salivales).
La permeabilidad depende de tres factores:
Tamaño de la molécula. - Polaridad/carga.
- Liposolubilidad.
A mayor liposolubilidad y menor tamaño, mayor permeabilidad por difusión simple.
4.3. Clasificación general del transporte de membrana
El transporte de sustancias a través de la membrana se clasifica en función de dos criterios fundamentales: si requiere o no gasto energético (ATP) y si se realiza a favor o en contra de gradiente.
4.3.1. Transporte pasivo
Se produce a favor de gradiente (de concentración, eléctrico o electroquímico) y no requiere gasto de ATP. El soluto se mueve espontáneamente de donde hay más a donde hay menos.
4.3.1.1. Difusión simple
La difusión es el proceso de homogeneización de una sustancia desigualmente concentrada, producido como consecuencia exclusiva de la agitación térmica. La agitación térmica tiende a igualar concentraciones mediante un flujo de concentración (Φc), definido como el número de moles que por unidad de superficie y tiempo atraviesan una superficie perpendicular.
El flujo de difusión de una sustancia es proporcional al gradiente de concentración que lo provoca. Esta relación se expresa mediante la Ley de Fick:
Φc = −D · (dC/dx)
Donde D es el coeficiente de difusión: la relación entre el flujo de difusión de una sustancia y el gradiente de concentración que lo provoca. El coeficiente D aumenta con la temperatura y disminuye con el peso molecular del soluto.
Las moléculas atraviesan directamente la bicapa lipídica sin intervención de proteínas. Sin embargo, la membrana no es un medio homogéneo — es lipídica — lo que limita el paso de sustancias hidrófilas. Para describir el comportamiento real de la membrana se introduce el coeficiente de permeabilidad (P): el valor que debería tener el coeficiente de difusión si la membrana fuera homogénea para producir, ante la misma diferencia de concentración, el mismo flujo observado. La Ley de Fick modificada para membranas queda:
Φc = P · (C₁ − C₂)
Donde P depende de tres factores:
P = D · K / l
- D: coeficiente de difusión de la sustancia
- K: coeficiente de reparto — la proporción de soluto que se adsorbe a la membrana; aumenta con la liposolubilidad de la sustancia
- l: grosor de la membrana
La permeabilidad aumenta cuando:
- Aumenta D (a mayor temperatura, o menor peso molecular)
- Aumenta K (a mayor liposolubilidad)
- Disminuye l (menor grosor de membrana)
El equilibrio por difusión simple se alcanza cuando la concentración a ambos lados de la membrana es igual. Para volúmenes iguales: C₁final = C₂final (la concentración final es la media de ambas concentraciones iniciales).
Características de la difusión simple: no saturable, no específica, no regulable, cinética lineal.
4.3.1.2. Ósmosis
Es el movimiento neto de agua a través de una membrana semipermeable, desde la solución de menor osmolaridad (hipotónica) hacia la de mayor osmolaridad (hipertónica). El flujo fisiológico de agua en tejidos como el riñón depende en gran medida de acuaporinas (AQP1, AQP2).
4.3.1.3. Difusión facilitada
Requiere proteínas de membrana (canales o transportadores). A favor de gradiente y sin gasto de ATP, pero con dos subtipos:
| Propiedad | Canales iónicos | Transportadores (carriers) |
|---|---|---|
| Mecanismo | Poro acuoso que permite paso rápido de iones | Unión del soluto, cambio conformacional, liberación |
| Velocidad | Muy rápida (10⁶–10⁸ iones/s) | Más lenta (10²–10⁴ moléculas/s) |
| Selectividad | Alta para iones específicos | Alta para moléculas específicas |
| Saturabilidad | No saturable | Saturable (cinética tipo Michaelis-Menten) |
| Regulación | Voltaje, ligandos, mecánica | Expresión génica, fosforilación |
| Estados | Abierto / cerrado / inactivo | Dos conformaciones alternantes |
| Ejemplos | Na⁺, K⁺, Ca²⁺, Cl⁻ (voltaje-dep.); nAChR (ligando-dep.) | GLUT1-4 (glucosa), UT (urea) |
Canales iónicos: clasificación por mecanismo de apertura
| Tipo de canal | Activación | Ejemplos clave |
|---|---|---|
| Voltaje-dependiente | Cambio en el potencial de membrana (despolarización) | Nav (Na⁺), Kv (K⁺), Cav (Ca²⁺) |
| Ligando-dependiente | Unión de un neurotransmisor u otra molécula | nAChR (acetilcolina), GABA-A, NMDA (glutamato) |
| Mecanosensible | Estímulo mecánico (estiramiento, presión) | Piezo1, Piezo2 (tacto, barorreceptores) |
| De fuga (leak) | Permanentemente abierto (sin compuerta regulable) | K2P (TASK, TREK) – determinan el potencial de reposo |
- Los canales iónicos pueden estar en tres estados: abierto, cerrado e inactivo.
- Los canales de fuga (leak) no tienen compuerta regulable y están siempre abiertos.
- Difusión facilitada por transportadores: saturable y específica (cinética de Michaelis-Menten). Difusión simple: no saturable.
- Receptores ionotropos = canales ligando-dependientes. Receptores metabotropos = acoplados a proteína G.
4.3.2. Transporte activo
Gradiente electroquímico: gradiente neto resultante del gradiente de concentración y el gradiente de potencial eléctrico. Coincide con el sentido de ambos gradientes o con el del predominante, y define el sentido del flujo neto de un ión por causas exclusivamente físicas.
El transporte activo se produce en contra del gradiente electroquímico del soluto transportado. Cuando un ión se mueve en sentido contrario a su gradiente electroquímico, necesariamente se consume energía — directa o indirectamente derivada del ATP.
4.3.2.1. Transporte activo primario
La propia proteína transportadora posee actividad ATPasa: hidroliza directamente ATP para mover solutos en contra de gradiente. Se denominan genéricamente bombas.
Las bombas ATPasas se clasifican en cuatro tipos según su mecanismo:
- Tipo P (phosphorylation): el cambio conformacional se produce mediante fosforilación directa de la proteína. Ejemplos: Na⁺/K⁺ ATPasa, Ca²⁺ ATPasa (PMCA, SERCA), H⁺/K⁺ ATPasa.
- Tipo V (vacuolar): transportan H⁺ hacia vacuolas, lisosomas o endosomas. No interviene el fosfato como intermediario. Ejemplo: V-ATPasa.
- Tipo F (factor de acoplamiento): normalmente sintetizan ATP a partir del gradiente de H⁺ (ATP sintasa mitocondrial). Funcionan en sentido inverso al resto de bombas.
- Tipo ABC (ATP-binding cassette): utilizan la unión e hidrólisis de ATP en dominios citosólicos específicos. Ejemplos: MDR1 (resistencia a fármacos), CFTR (canal de Cl⁻, fibrosis quística).
| Bomba | Tipo | Estequiometría | Localización / Función |
|---|---|---|---|
| Na⁺/K⁺ ATPasa | P | 3 Na⁺ fuera, 2 K⁺ dentro / 1 ATP | Ubicua. Mantiene gradientes de Na⁺ y K⁺. Electrogénica. |
| Ca²⁺ ATPasa (PMCA) | P | 2 Ca²⁺ fuera / 1 ATP | Membrana plasmática. Mantiene [Ca²⁺]i muy baja (~100 nM). |
| Ca²⁺ ATPasa (SERCA) | P | 2 Ca²⁺ al retículo / 1 ATP | Retículo endoplásmico/sarcoplásmico. Relajación muscular. |
| H⁺/K⁺ ATPasa | P | H⁺ fuera, K⁺ dentro / 1 ATP | Células parietales gástricas. Secreción de HCl. |
| H⁺ ATPasa (V-ATPasa) | V | H⁺ al lumen / 1 ATP | Lisosomas, endosomas. Acidificación. |
| ATP sintasa | F | Funciona en sentido inverso: sintetiza ATP | Mitocondrias (membrana interna). Fosforilación oxidativa. |
| Superfamilia ABC | ABC | Variable | MDR1 (resistencia a fármacos), CFTR (Cl⁻, fibrosis quística). |
La bomba Na⁺/K⁺ ATPasa
Es la bomba más importante de las células animales. Consume hasta el 30-40% del ATP total de la célula (y hasta el 70% en las neuronas). Está formada por dos subunidades principales: α (catalítica, con actividad ATPasa y sitios de unión para Na⁺, K⁺ y ouabaína) y β (reguladora, necesaria para el correcto plegamiento y tráfico a membrana). Existen isoformas α1-α4 con distribución tisular específica.
Los gradientes iónicos que genera la bomba Na⁺/K⁺ ATPasa son la base física del potencial de membrana en reposo que determina la excitabilidad de neuronas y células musculares.
Este aspecto se desarrolla en el T9 – Propiedades de la membrana en reposo.
La bomba Na⁺/K⁺ es electrogénica (saca 3 cargas positivas y mete 2: carga neta = –1), contribuyendo con ~–3 a –5 mV al potencial de membrana en reposo. La ouabaína es su inhibidor clásico.
La bomba de Ca²⁺
La concentración de Ca²⁺ intracelular se mantiene extremadamente baja (~100 nM frente a ~1-2 mM en el exterior), un gradiente de 10.000:1. Las bombas de Ca²⁺ son de tipo P y poseen sitios de unión de alta afinidad en el lado citosólico. Bombean 2 Ca²⁺ por ATP hidrolizado. Son esenciales para:
- La relajación muscular (SERCA en el retículo sarcoplásmico).
- Finalización de la señalización por Ca²⁺ (cascadas intracelulares).
- Prevención de la apoptosis (un exceso de Ca²⁺ citosólico activa caspasas).
Excepción energética
Como excepción, algunos sistemas de transporte activo obtienen la energía a partir de reacciones de oxidación-reducción (redox), no de la hidrólisis de ATP. Es el caso de algunas bombas de protones en bacterias y mitocondrias, donde el gradiente electroquímico se genera acoplado a la cadena de transporte electrónico.
4.3.2.2. Transporte activo secundario
No utiliza ATP directamente. Aprovecha el gradiente electroquímico de un ión (generalmente Na⁺, creado por la bomba Na⁺/K⁺) para transportar otro soluto en contra de su gradiente. Existen dos modalidades:
| Modalidad | Dirección | Ejemplo | Función |
|---|---|---|---|
| Simporte (cotransporte) | Ambas sustancias en el mismo sentido | SGLT1 (Na⁺ + glucosa → interior) | Absorción intestinal de glucosa |
| NKCC1 (Na⁺/K⁺/2Cl⁻ → interior) | Secreción ep. y regulación de volumen | ||
| Antiporte (contratransporte) | Sustancias en sentido opuesto | NCX (3 Na⁺ → int / 1 Ca²⁺ → ext) | Regulación de Ca²⁺ cardíaco |
| NHE (Na⁺ → int / H⁺ → ext) | Regulación del pH intracelular |
- Transporte activo primario: la proteína hidroliza ATP directamente (bombas ATPasas).
- Transporte activo secundario: usa el gradiente creado por una bomba (generalmente el gradiente de Na⁺ de la Na⁺/K⁺ ATPasa).
- SGLT1: simporte Na⁺-glucosa en intestino. GLUT: difusión facilitada de glucosa (pasivo). Distinción frecuente en examen.
- NCX (intercambiador Na⁺/Ca²⁺): 3Na⁺:1Ca²⁺. Crítico en el miocardio. Diana de fármacos cardíacos.
4.3.3. Transporte vesicular
Para macromoléculas y partículas grandes que no pueden atravesar la membrana ni siquiera mediante proteínas transportadoras, la célula utiliza vesículas de membrana. Requiere ATP y el sistema de citoesqueleto.
| Tipo | Dirección | Subtipos | Ejemplo |
|---|---|---|---|
| Endocitosis | Exterior → interior | Fagocitosis (partículas grandes) | — |
| Pinocitosis (líquidos) | |||
| Endocitosis mediada por receptor (específica) | LDL (receptor LDL), hierro (transferrina) | ||
| Exocitosis | Interior → exterior | Constitutiva o regulada | Neurotransmisores (regulada), mucina (constitutiva) |
| Transcitosis | Polo apical → basal (o viceversa) | Combinación endocitosis + exocitosis | IgA en epitelio intestinal; albúmina en endotelio; paso de macromoléculas en la barrera hematoencefálica |
La endocitosis mediada por receptor es el mecanismo más eficiente y específico de internalización de macromoléculas. Utiliza fosas cubiertas de clatrina. Defectos en el receptor de LDL causan hipercolesterolemia familiar.
4.4. Relevancia clínica del transporte de membrana
Los mecanismos de transporte de membrana son dianas terapéuticas fundamentales en medicina. Muchos fármacos actúan modulando canales, bombas o transportadores:
| Patología / Fármaco | Diana | Mecanismo |
|---|---|---|
| Fibrosis quística | CFTR (canal Cl⁻, familia ABC) | Mutación ΔF508 impide el tráfico a membrana. Fcos. correctores: ivacaftor, lumacaftor. |
| Digoxina (ICC) | Na⁺/K⁺ ATPasa | Inhibe la bomba → ↑Na⁺i → NCX invierte → ↑Ca²⁺i → ↑fuerza contráctil cardíaca. |
| Omeprazol (ERGE) | H⁺/K⁺ ATPasa gástrica | Inhibidor irreversible de la bomba de protones → reduce secreción ácida. |
| Gliflozinas (DM2) | SGLT2 (túbulo renal) | Inhiben reabsorción renal de glucosa → glucosuria → reduce glucemia. |
| Lidocaína (anestesia) | Canales Nav (voltaje-dep.) | Bloquea canales de Na⁺ → impide potenciales de acción → analgesia local. |
| Diabetes insípida nefrogénica | AQP2 (acuaporina renal) | Defecto en la respuesta a ADH → no se insertan AQP2 → poliuria. |
- CFTR es un canal de Cl⁻ de la superfamilia ABC. La mutación más común en fibrosis quística es ΔF508.
- La digoxina inhibe la Na⁺/K⁺ ATPasa: efecto inotrópico positivo en insuficiencia cardíaca.
- SGLT2 es transporte activo secundario (simporte Na⁺-glucosa) en túbulo proximal renal.
- Los inhibidores de la bomba de protones (IBP) actúan sobre la H⁺/K⁺ ATPasa de las células parietales.
